Una nueva mirada a cómo los químicos en la luna Europa de Júpiter pueden estar reaccionando juntos podría proporcionar una nueva visión de cómo podrían estar ocurriendo las reacciones químicas en la corteza helada de la luna, a pesar de las frías temperaturas. Debido a que la reacción ocurre sin la ayuda de la radiación, podría tener lugar a través de la gruesa capa de hielo de Europa. Si esto está ocurriendo, renovaría el pensamiento actual sobre la química y la geología de esta luna y quizás de otras.
Europa tiene temperaturas alrededor de 86 a 130 Kelvin (menos 300 a menos 225 grados Fahrenheit), y en esas condiciones extremadamente frías, la mayoría de las reacciones químicas requieren una infusión de energía de la radiación o la luz. En Europa, la energía proviene de partículas de los cinturones de radiación de Júpiter. Debido a que la mayoría de esas partículas penetran solo fracciones de una pulgada en la superficie, los modelos de la química de Europa generalmente se detienen allí.
"Cuando las personas hablan de química en Europa, generalmente hablan de reacciones que son impulsadas por la radiación", dice el científico de Goddard Reggie Hudson. "Una vez que te pones debajo de la superficie de Europa, hace frío y es sólido, y normalmente no esperas que las cosas sucedan muy rápido en esas condiciones", dijo Reggie Hudson, del Laboratorio de Astroquímica de Goddard de la NASA.
"Pero con la química que describimos", dijo Mark Loeffler, primer autor del artículo publicado en Geophysical Research Letters, "podría tener hielo de 10 o 100 metros [aproximadamente 33 o 330 pies] de espesor, y si tiene azufre mezclado con dióxido, vas a tener una reacción ".
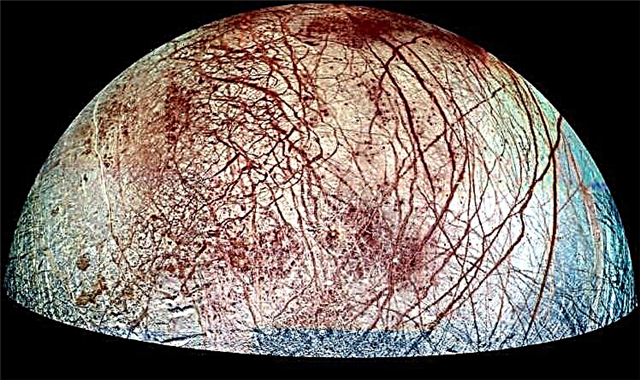
La espectroscopía muestra que hay azufre en el hielo de Europa, y los astrónomos creen que se origina en los volcanes de la luna Io de Júpiter, luego se ioniza y se transporta a Europa, donde se incrusta en el hielo. Pero originalmente, los astrónomos pensaron que no podría ocurrir una gran reacción entre el hielo de agua y el azufre.
Loeffler y Hudson rociaron vapor de agua y gas de dióxido de azufre en espejos de un cuarto de tamaño en una cámara de alto vacío. Debido a que los espejos se mantuvieron a aproximadamente 50 a 100 Kelvin (aproximadamente menos 370 a menos 280 grados Fahrenheit), los gases se condensaron inmediatamente como hielo. A medida que avanzaba la reacción, los investigadores utilizaron espectroscopía infrarroja para observar la disminución de las concentraciones de agua y dióxido de azufre y el aumento de las concentraciones de iones positivos y negativos generados.
Incluso con las temperaturas extremadamente frías, las moléculas reaccionaron rápidamente en sus formas heladas. "A 130 Kelvin [aproximadamente menos 225 grados Fahrenheit], que representa el extremo cálido de las temperaturas esperadas en Europa, esta reacción es esencialmente instantánea", dijo Loeffler. “A 100 Kelvin, puedes saturar la reacción después de medio día a un día. Si eso no suena rápido, recuerde que en escalas de tiempo geológicas, miles de millones de años, un día es más rápido que un abrir y cerrar de ojos ".
Para probar la reacción, los investigadores agregaron dióxido de carbono congelado, también conocido como hielo seco, que se encuentra comúnmente en cuerpos helados, incluido Europa. "Si el dióxido de carbono congelado hubiera bloqueado la reacción, no estaríamos tan interesados", dijo Hudson, "porque entonces la reacción probablemente no sería relevante para la química de Europa". Sería una curiosidad de laboratorio. Pero la reacción continuó, lo que significa que podría ser importante tanto en Europa como en Ganímedes y Calisto, dos lunas más de Júpiter y otros lugares donde están presentes tanto el agua como el dióxido de azufre.
La reacción convirtió un cuarto en casi un tercio del dióxido de azufre en diferentes productos. "Este es un rendimiento inesperadamente alto para esta reacción química", dijo Loeffler. "Hubiéramos estado contentos con el cinco por ciento".
Además, los iones positivos y negativos producidos reaccionarán con otras moléculas. Esto podría conducir a una química intrigante, especialmente porque el bisulfito, un tipo de ion azufre, y algunos otros productos de esta reacción son lo suficientemente resistentes al refractario como para durar bastante tiempo.
Este nuevo hallazgo inducirá nuevas observaciones remotas de Europa para ver si se puede encontrar evidencia de algún producto basado en la reacción.
Fuente: JPL